En mayo, un hombre de edad avanzada fue internado en el hospital Monte Sinaí de Brooklyn para una intervención quirúrgica en el abdomen. Una prueba de sangre reveló que estaba infectado con un germen recién descubierto, tan mortal como misterioso.
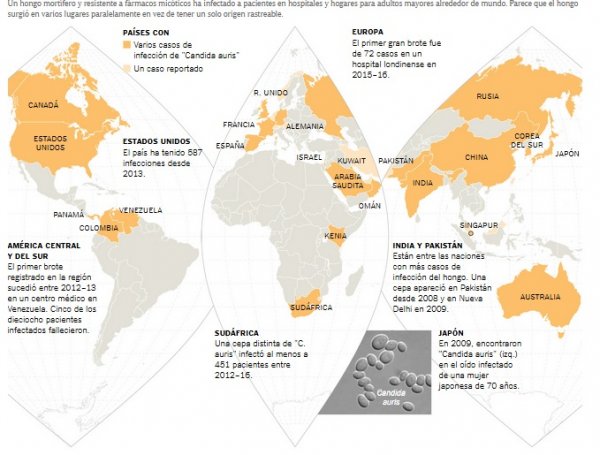
Era un hongo llamado Candida auris, el cual ataca a la gente que tiene un sistema inmunitario debilitado y se está propagando en silencio por todo el mundo. En los últimos cinco años ha sido reportado en una unidad neonatal en Venezuela, se esparció por un hospital en España, forzó a un centro médico prestigioso en el Reino Unido a cerrar su unidad de cuidados intensivos y se han observado casos en India, Pakistán y Sudáfrica.
Recientemente, C. auris llegó a Nueva York, Nueva Jersey e Illinois, por lo cual los Centros para el Control y la Prevención de Enfermedades (CDC) lo añadieran a una lista de gérmenes clasificados como “amenazas inmediatas”.
El anciano en Monte Sinaí murió en ese hospital después de noventa días de hospitalización, pero C. auris subsistió. Las pruebas lo detectaron en todos los rincones de su habitación, en una forma tan invasiva que el hospital requirió de un equipo especial de limpieza y tuvo que quitar parte de las losetas del piso y el techo para erradicarlo.
En parte, C. auris es así de tenaz porque no responde a los principales fármacos antimicóticos; un nuevo ejemplo de una de las amenazas a la salud más intratables del mundo: la aparición de infecciones resistentes a los medicamentos.
Durante décadas, los especialistas en salud pública han advertido que el uso indiscriminado de antibióticos está disminuyendo su eficacia, que han aumentado la expectativa de vida por su capacidad para curar infecciones bacterianas que alguna vez fueron comúnmente mortales; pero, también ha habido un auge de hongos resistentes a los medicamentos.
“Es un problema enorme”, señaló Matthew Fisher, profesor de Epidemiología de las Enfermedades Fúngicas en el Imperial College London (Escuela Imperial de Londres) y autor de un estudio reciente sobre la resistencia de los hongos a los fármacos. “Dependemos de poder tratar a esos pacientes con antimicóticos”.
En términos sencillos, los hongos, al igual que las bacterias, están desarrollando defensas para sobrevivir a los medicamentos modernos.
Estas llamadas superbacterias o supergérmenes tienen mayor letalidad entre personas con sistemas inmunitarios no desarrollados o comprometidos, como los de los recién nacidos, ancianos, fumadores, diabéticos y personas con ciertas enfermedades autoinmunes. Los especialistas alertan de que, a menos que se desarrollen nuevos fármacos efectivos y se ataje el uso de medicamentos antimicóticos cuando son innecesarios, el riesgo mortífero de estos hongos y bacterias resistentes se expandirá a poblaciones más saludables.
Un estudio financiado por el gobierno británico calcula que si no se establecen políticas para frenar el aumento de la resistencia a los medicamentos, en 2050 podrían morir diez millones de personas en todo el mundo a causa de esas infecciones. Esa cifra supera los ocho millones de personas que se calcula morirán de cáncer este 2019. En la actualidad, las muertes por infecciones resistentes a los medicamentos rondan los 700.000 fallecimientos.
Los antibióticos y antimicóticos son esenciales para combatir las infecciones que contraen las personas, pero los antibióticos también se emplean para prevenir enfermedades en los animales de granja, mientras que los antimicóticos se aplican además para evitar que se pudran los cultivos agrícolas. Algunos científicos indican que el uso cada vez mayor de herbicidas y fungicidas en los cultivos está contribuyendo a la aparición de hongos resistentes a los medicamentos entre seres humanos que consumen esos cultivos.
A pesar de que el problema está aumentando, hay poco conocimiento por parte de la población, en parte debido a que la existencia de infecciones resistentes con frecuencia se mantiene en secreto. Los hospitales y los gobiernos locales son renuentes a publicar la aparición de los brotes, tanto de bacterias como de hongos, por temor a que los consideren focos de infección.
Mientras, los gérmenes se esparcen entre pacientes y personal de salud en los hospitales o con el equipo médico; son transportados en la carne y vegetales fertilizados por estiércol de las granjas que usan los antibióticos, y cruzan fronteras por medio de viajeros y en las exportaciones e importaciones.
C. auris, que infectó al hombre hospitalizado en el hospital Monte Sinaí, es uno de decenas de bacterias y hongos peligrosos que han desarrollado resistencia.
Otras cepas destacadas del hongo Candida -uno de los causantes más comunes de las infecciones en el torrente sanguíneo que se presentan en los hospitales- no han desarrollado una resistencia importante a los fármacos, pero los CDC indican que más del 90 por ciento de las infecciones causadas por C. auris son resistentes al menos a un medicamento y el 30 por ciento son resistentes a dos o más fármacos.
Según los CDC, casi la mitad de los pacientes que contraen C. auris fallecen en noventa días. No obstante, los especialistas a nivel mundial no han determinado de dónde vino en primera instancia.
“Es una criatura de la laguna negra”, señaló Tom Chiller, director del departamento dedicado a los hongos en el CDC. “Surgió en algún sitio y ahora está en todas partes”.
Brotes silenciados
A finales de 2015, Johanna Rhodes, especialista en enfermedades infecciosas del Imperial College London, recibió una llamada de emergencia del Royal Brompton Hospital, en las afueras de Londres. El C. auris llevaba meses instalado ahí y el hospital no podía deshacerse de él.
“No tenemos idea de dónde viene. Nunca hemos escuchado de él. Solo se extendió como el fuego”, recordó Rhodes que le dijeron. Aceptó ayudar al hospital a identificar el perfil genético del hongo y eliminarlo de las habitaciones. Sugirió usar un aparato especial para rociar peróxido de hidrógeno en aerosol en la habitación que fue usada por un paciente con C. auris, con la teoría de que el vapor eliminaría el hongo de todas las esquinas. El aparato rociador estuvo prendido durante una semana. Luego pusieron una placa con gel para que atrajera a cualquier microbio aún existente y que ese creciera ahí, dijo Rhodes.
El único organismo que seguía presente era C. auris.
Se estaba propagando, pero no se dijo nada fuera del hospital. El Royal Brompton, centro especializado en padecimientos del pulmón y del corazón a donde llegan también pacientes adinerados de Medio Oriente y de toda Europa, alertó al gobierno británico y les informó a los pacientes infectados, pero no hizo declaraciones públicas.
Este pánico silenciado se está volviendo la norma en los hospitales de todo el mundo. Las instituciones y los gobiernos nacionales, estatales y locales se han mostrado renuentes a divulgar la presencia de los brotes de las infecciones resistentes con el argumento de que no tiene caso asustar a los pacientes actuales… ni a los futuros pacientes.
Silke Schelenz, infectóloga en el Royal Brompton, consideró “muy muy frustrante” la falta de celeridad por parte del gobierno y del hospital en las primeras etapas del brote.
“Evidentemente, no querían perder su buena reputación”, señaló Schelenz. “No había afectado nuestros resultados quirúrgicos”.
Para finales de junio de 2016, un artículo publicado en una revista científica informó acerca de “un brote en curso de cincuenta casos de C. auris” en el Royal Brompton y el hospital tomó una medida extraordinaria: cerró su sala de terapia intensiva durante once días. Una vez más, sin hacer ninguna declaración.
Unos días después, el hospital finalmente reconoció el problema al hablar con un periódico. El encabezado de The Daily Telegraph advertía: “Sala de terapia intensiva cerrada tras la aparición de un nuevo y mortal supergermen en el Reino Unido”.
Sin embargo, poco se supo del asunto a nivel internacional, aunque ya había comenzado un brote incluso más grande en Valencia, España, en el Hospital Universitario y Politécnico de La Fe. Al igual que el Royal Brompton, este hospital español no emitió ningún comunicado. A la fecha, aún no lo ha hecho.
El secretismo indigna a defensores de los derechos de pacientes, quienes afirman que la gente tiene derecho a saber si existe algún brote para decidir si visitar un hospital para algún problema que no sea de urgencia, como una intervención electiva. “¿Por qué diablos estamos leyendo sobre un brote casi un año y medio después y no está en las primeras planas al día siguiente de que ocurre?”, comentó Kevin Kavanagh, presidente de Health Watch USA, una organización sin fines de lucro para la defensa de los pacientes.
Los funcionarios de salud señalan que publicar la presencia de brotes atemoriza a los pacientes respecto a una situación acerca de la cual no pueden hacer nada, en especial cuando los riesgos no son claros. “Ya es lo suficientemente difícil para los especialistas en atención médica descifrar estos organismos”, comentó Anna Yaffee, quien trabajaba en los CDC como investigadora en materia de brotes. “En verdad es imposible comunicarlo a la población”.
Los funcionarios de Londres sí alertaron a los CDC sobre el brote en el Royal Brompton cuando estaba ocurriendo. Los funcionarios en CDC se percataron de que tenían que difundir esa información a los hospitales de Estados Unidos. El 24 de junio de 2016, CDC lanzó una advertencia a todo el país y abrió una cuenta de correo electrónico, candidaauris@cdc.gov, para recibir preguntas. Snigdha Vallabhaneni, integrante clave del equipo especialista en hongos, dijo que esperaba recibir muy pocos comentarios, “tal vez un mensaje al mes”.
No obstante, a las pocas semanas, su buzón reventó. Según CDC, tan solo en Estados Unidos se había informado de 587 casos de personas que habían contraído el C. auris. Los síntomas -fiebre, dolor y fatiga- aparentemente son comunes, pero cuando una persona se infecta, en especial si ya tiene un sistema inmunitario débil, esos síntomas comunes pueden ser letales.
¿Qué tanto afectan los pesticidas?
Debido a que CDC trabaja para restringir la propagación del C. auris resistente a los medicamentos, sus investigadores han estado intentando responder a esta inquietante pregunta: ¿en qué parte del mundo surgió?
La primera vez que los médicos se encontraron con C. auris fue en 2009 en Japón: estaba en el oído de una mujer (auris quiere decir oído en latín). En ese momento parecía un primo inocuo de las infecciones micóticas comunes y fácilmente tratables. Tres años después, apareció en Nijmegen, en los Países Bajos, en un resultado poco común de una prueba en el laboratorio del microbiólogo Jacques Meis, quien estaba analizando una infección en el torrente sanguíneo de dieciocho pacientes procedentes de cuatro hospitales de India. Pronto empezaron a surgir cada mes nuevos grupos de C. auris en diferentes partes del mundo.
Cuando los investigadores de CDC compararon el genoma entero de muestras de Candida auris de India, Pakistán, Venezuela, Sudáfrica y Japón, descubrieron que su origen no era de un solo lugar y que no había solo una cepa de auris. La secuencia del genoma mostró que había cuatro versiones diferentes del hongo, con diferencias tan grandes que indicaban que estas cepas se habían separado hacía miles de años y que habían surgido como patógenos resistentes de cepas inofensivas del medioambiente en cuatro lugares diferentes al mismo tiempo.
“De alguna manera, dio un salto casi de manera simultánea y al parecer se propagó ya resistente a los fármacos, lo que en verdad es asombroso”, comentó Vallabhaneni.
Existen diferentes teorías sobre lo que sucedió con C. auris. Meis, el investigador neerlandés que registró el hongo en 2012, señaló que él pensaba que los hongos resistentes a los medicamentos se estaban desarrollando debido al uso excesivo de fungicidas en los cultivos.
A Meis le interesaron los hongos resistentes cuando escuchó sobre el caso de un paciente en los Países Bajos de 63 años que falleció en 2005 a causa del hongo Aspergillus. Se comprobó que era resistente a un tratamiento antimicótico de vanguardia llamado itraconazol. Ese fármaco es prácticamente una copia de los pesticidas de azol que se espolvorean en los cultivos de todo el mundo.
Chiller, el encargado del departamento de hongos del CDC, alberga la teoría de que quizá el C. auris se aprovechó del uso excesivo de los fungicidas. Tiene la idea de que el hongo en realidad ha existido durante miles de años, pero que no era un germen especialmente agresivo. Sin embargo, a medida que los azoles empezaron a destruir hongos más comunes, llegó la oportunidad de C. auris para llenar el vacío.
Sigue sin resolverse el misterio del origen del Candida auris y parece que, por el momento, su procedencia es menos importante que detener su propagación.